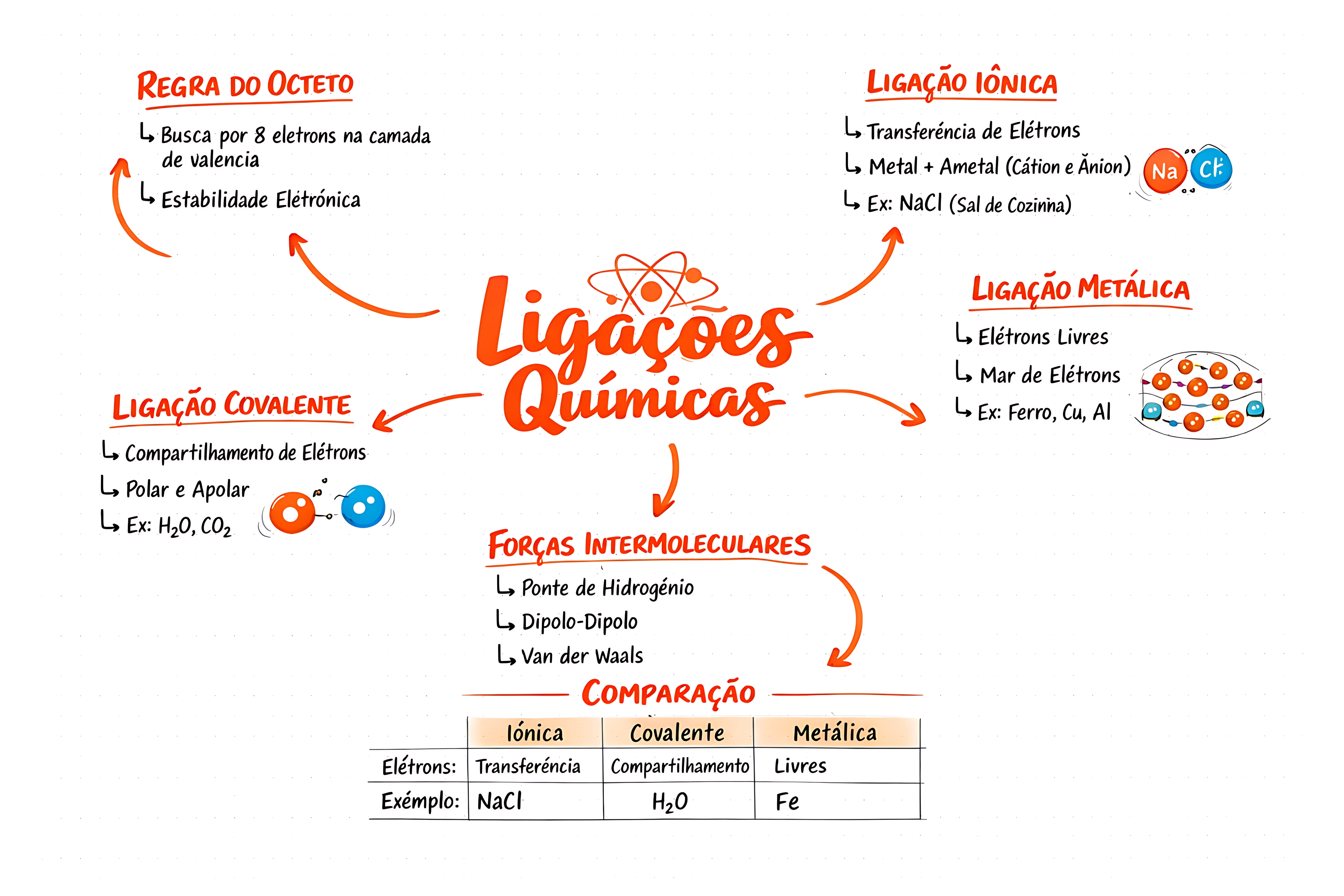
📌 O que são ligações químicas?
As ligações químicas são forças de atração que mantêm os átomos unidos, permitindo a formação de moléculas, substâncias simples e compostos químicos. Elas surgem a partir das interações entre os elétrons da camada de valência dos átomos.
Essas ligações são responsáveis por:
- A estrutura da matéria
- As propriedades físicas (estado físico, dureza, condutividade)
- As propriedades químicas (reatividade, polaridade, solubilidade)
Sem as ligações químicas, os átomos permaneceriam isolados, impossibilitando a existência da matéria como a conhecemos.
⚛️ Regra do octeto e estabilidade eletrônica
A maioria dos átomos tende a atingir uma configuração eletrônica semelhante à dos gases nobres, que possuem 8 elétrons na camada de valência (exceto o hélio, com 2).
➡️ Essa tendência é chamada de regra do octeto.
Para atingir essa estabilidade, os átomos podem:
- Perder elétrons
- Ganhar elétrons
- Compartilhar elétrons
Esses processos originam os diferentes tipos de ligações químicas.
⚠️ Importante: a regra do octeto possui exceções, como:
- Hidrogênio
- Elementos do 3º período em diante (expansão do octeto)
🧪 Principais tipos de ligações químicas
🔹 1. Ligação Iônica (ou eletrovalente)
A ligação iônica ocorre quando há transferência total de elétrons de um átomo para outro, formando íons com cargas opostas que se atraem eletrostaticamente.
📍 Onde ocorre?
- Entre metais (eletropositivos)
- ametais (eletronegativos)
O metal perde elétrons e forma um cátion (+), enquanto o ametal ganha elétrons e forma um ânion (−).
📘 Exemplo clássico:
- NaCl (cloreto de sódio)
🧊 Estrutura cristalina
Os compostos iônicos não formam moléculas isoladas, mas sim retículos cristalinos, com íons organizados de forma regular.
🔍 Propriedades da ligação iônica:
- Alto ponto de fusão e ebulição
- Geralmente sólidos à temperatura ambiente
- Conduzem eletricidade quando fundidos ou dissolvidos em água
- Muitos são solúveis em água
🔹 2. Ligação Covalente
A ligação covalente ocorre quando há compartilhamento de pares de elétrons entre átomos, geralmente ametais.
Essa ligação acontece quando a diferença de eletronegatividade entre os átomos é pequena.
📘 Exemplos:
- H₂O (água)
- CO₂ (gás carbônico)
- O₂ (oxigênio molecular)
📌 Tipos de ligação covalente
🔸 a) Quanto ao número de pares compartilhados
- Ligação simples → 1 par de elétrons
- Ligação dupla → 2 pares
- Ligação tripla → 3 pares
🔸 b) Quanto à polaridade
✔️ Ligação covalente apolar
Ocorre quando os átomos têm eletronegatividades iguais ou muito próximas.
📘 Exemplo:
- O₂, N₂
✔️ Ligação covalente polar
Ocorre quando há diferença de eletronegatividade, gerando polos positivo (δ⁺) e negativo (δ⁻).
📘 Exemplo:
- H₂O
🔍 Propriedades das substâncias covalentes:
- Baixo ponto de fusão (na maioria)
- Podem ser sólidas, líquidas ou gasosas
- Não conduzem eletricidade
- Formam moléculas bem definidas
🔹 3. Ligação Metálica
A ligação metálica ocorre entre átomos de metais. Nesse tipo de ligação, os elétrons da camada de valência não pertencem a um átomo específico, formando um mar de elétrons livres.
Esses elétrons se movimentam livremente entre os cátions metálicos.
📘 Exemplos:
- Ferro (Fe)
- Cobre (Cu)
- Alumínio (Al)
🔍 Propriedades explicadas pela ligação metálica:
- Alta condutividade elétrica
- Alta condutividade térmica
- Maleabilidade (formar lâminas)
- Ductilidade (formar fios)
- Brilho metálico
🧲 Forças intermoleculares (interações químicas)
Além das ligações químicas, existem forças intermoleculares, que são mais fracas, mas fundamentais.
Principais tipos:
- Ligação de hidrogênio
- Dipolo-dipolo
- Forças de London
📌 Elas explicam:
- Ponto de ebulição
- Solubilidade
- Estado físico das substâncias
⚠️ Importante: não são ligações químicas, mas interações entre moléculas.
📊 Comparação completa entre os tipos de ligações químicas
| Tipo | Elétrons | Ocorre entre | Estrutura | Exemplo |
|---|---|---|---|---|
| Iônica | Transferência | Metal + Ametal | Retículo cristalino | NaCl |
| Covalente | Compartilhamento | Ametais | Moléculas | H₂O |
| Metálica | Elétrons livres | Metais | Rede metálica | Fe |
🧠 Importância das ligações químicas
O estudo das ligações químicas é essencial para compreender:
- Reações químicas
- Biologia molecular
- Materiais industriais
- Processos ambientais
- Química orgânica e inorgânica
É um dos temas mais cobrados em:
- ENEM
- Vestibulares
- Ensino Médio e Fundamental
📚 Conclusão
As ligações químicas são a base da Química e explicam como os átomos se unem para formar toda a matéria existente. Compreender suas características, tipos e propriedades permite entender o funcionamento do mundo microscópico e suas aplicações no cotidiano.