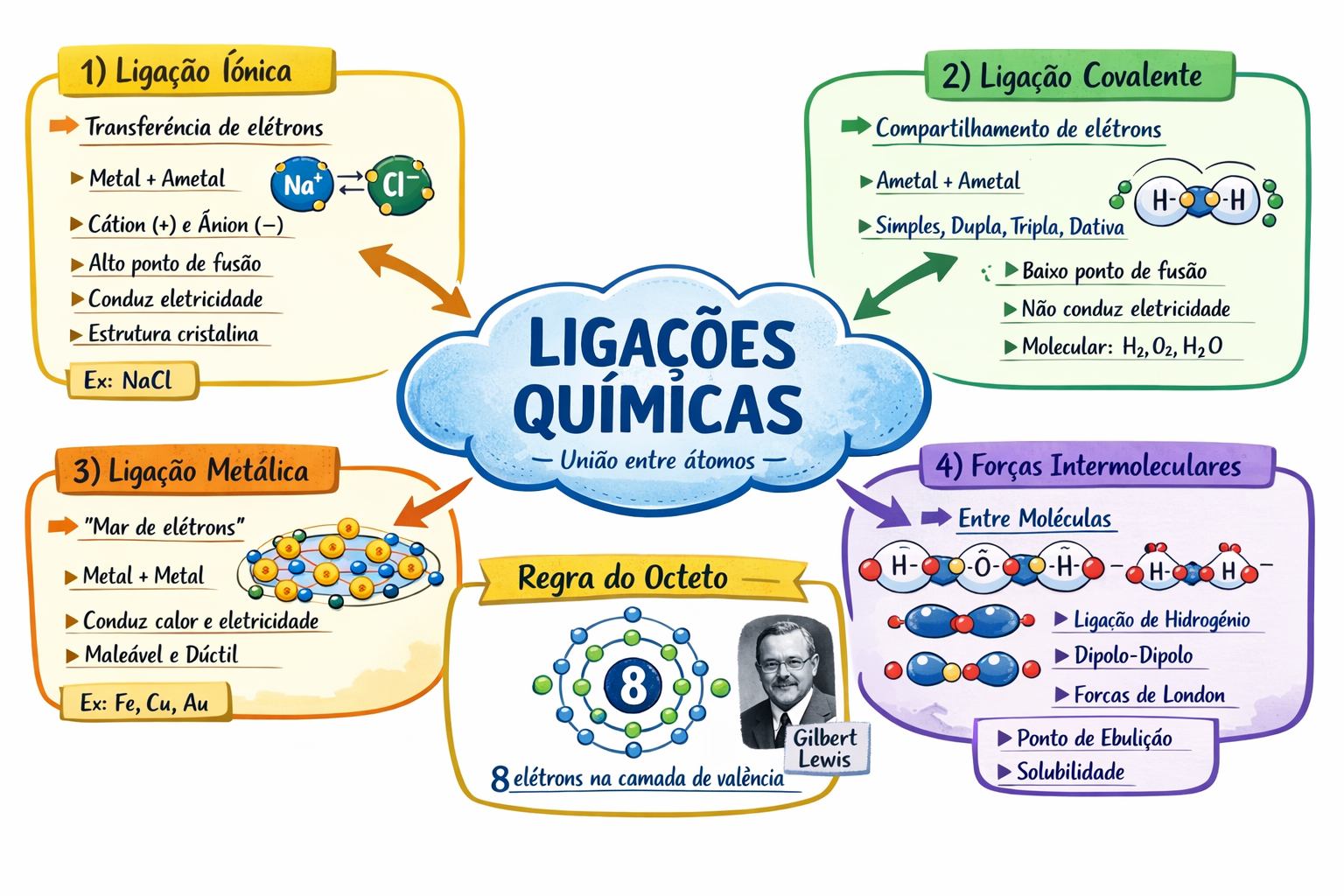
As ligações químicas são as forças de atração que mantêm os átomos unidos, formando moléculas e compostos. Essenciais para a existência de toda a matéria, essas interações ocorrem porque os átomos buscam alcançar uma configuração eletrônica mais estável, geralmente similar à dos gases nobres, que possuem oito elétrons em sua camada de valência (a camada mais externa) . Este fenômeno é amplamente explicado pela Regra do Octeto.
O que são Ligações Químicas e Por Que Ocorrem?
Os átomos, em seu estado natural, podem ser instáveis devido à sua configuração eletrônica. Para atingir a estabilidade, eles interagem uns com os outros, seja doando, recebendo ou compartilhando elétrons. Essas interações resultam na formação de ligações químicas, que são a base para a formação de todas as substâncias que conhecemos .
A Regra do Octeto e a Estabilidade Atômica
A Regra do Octeto é um princípio fundamental que guia a formação das ligações químicas. Ela postula que os átomos tendem a se ligar de forma a completar oito elétrons em sua camada de valência, tornando-se assim mais estáveis. Embora existam exceções (como o dueto para o hidrogênio e hélio, octeto incompleto e expansão do octeto), a regra do octeto é um excelente modelo para entender a maioria das ligações .
Tipos Principais de Ligações Químicas
Existem três tipos principais de ligações químicas, classificadas de acordo com a natureza dos átomos envolvidos e a forma como os elétrons são transferidos ou compartilhados:
1. Ligação Iônica (Eletrovalente)
A ligação iônica ocorre geralmente entre um metal (que tende a perder elétrons, formando cátions) e um ametall (que tende a ganhar elétrons, formando ânions). Há uma transferência definitiva de elétrons de um átomo para outro, resultando na formação de íons com cargas opostas que se atraem eletrostaticamente .
•Características: Formam compostos iônicos, que são sólidos cristalinos, possuem altos pontos de fusão e ebulição, e conduzem corrente elétrica quando fundidos ou dissolvidos em água.
•Exemplo: Cloreto de Sódio (NaCl). O Sódio (Na) doa um elétron para o Cloro (Cl), formando Na⁺ e Cl⁻.
2. Ligação Covalente (Molecular)
A ligação covalente ocorre principalmente entre ametais (ou entre um ametal e o hidrogênio), onde há compartilhamento de elétrons para que ambos os átomos atinjam a estabilidade. Os elétrons compartilhados pertencem simultaneamente à camada de valência de ambos os átomos .
•Características: Formam moléculas. Podem ser sólidos, líquidos ou gases à temperatura ambiente, com pontos de fusão e ebulição geralmente mais baixos que os compostos iônicos. Não conduzem corrente elétrica (com exceções).
•Exemplo: Água (H₂O). Cada átomo de Hidrogênio compartilha um par de elétrons com o Oxigênio.
Ligação Covalente Dativa (Coordenada)
Um tipo especial de ligação covalente é a ligação covalente dativa (ou coordenada), onde um dos átomos fornece o par de elétrons que será compartilhado. Ocorre quando um átomo já atingiu o octeto, mas ainda possui pares de elétrons não ligantes que podem ser compartilhados com outro átomo que precisa de elétrons .
3. Ligação Metálica
A ligação metálica ocorre entre átomos de metais. Caracteriza-se pela formação de um “mar de elétrons” deslocalizados, onde os elétrons da camada de valência não pertencem a um átomo específico, mas se movem livremente entre todos os átomos metálicos. Essa nuvem eletrônica mantém os íons metálicos positivos unidos .
•Características: Responsável pelas propriedades típicas dos metais, como alta condutividade elétrica e térmica, maleabilidade, ductilidade e brilho metálico. Formam ligas metálicas.
•Exemplo: Cobre (Cu), Ferro (Fe), ligas como o bronze (Cobre + Estanho).
Comparativo dos Tipos de Ligações Químicas
| Característica | Ligação Iônica | Ligação Covalente | Ligação Metálica |
| Átomos Envolvidos | Metal + Ametal | Ametal + Ametal (ou H) | Metal + Metal |
| Mecanismo | Transferência de elétrons | Compartilhamento de elétrons | Mar de elétrons deslocalizados |
| Estado Físico (T.A.) | Sólido | Sólido, Líquido ou Gás | Sólido |
| Condutividade Elétrica | Fundido/Dissolvido | Não condutor (geralmente) | Ótimo condutor |
| Exemplo | NaCl | H₂O, O₂ | Cu, Fe |
Importância das Ligações Químicas
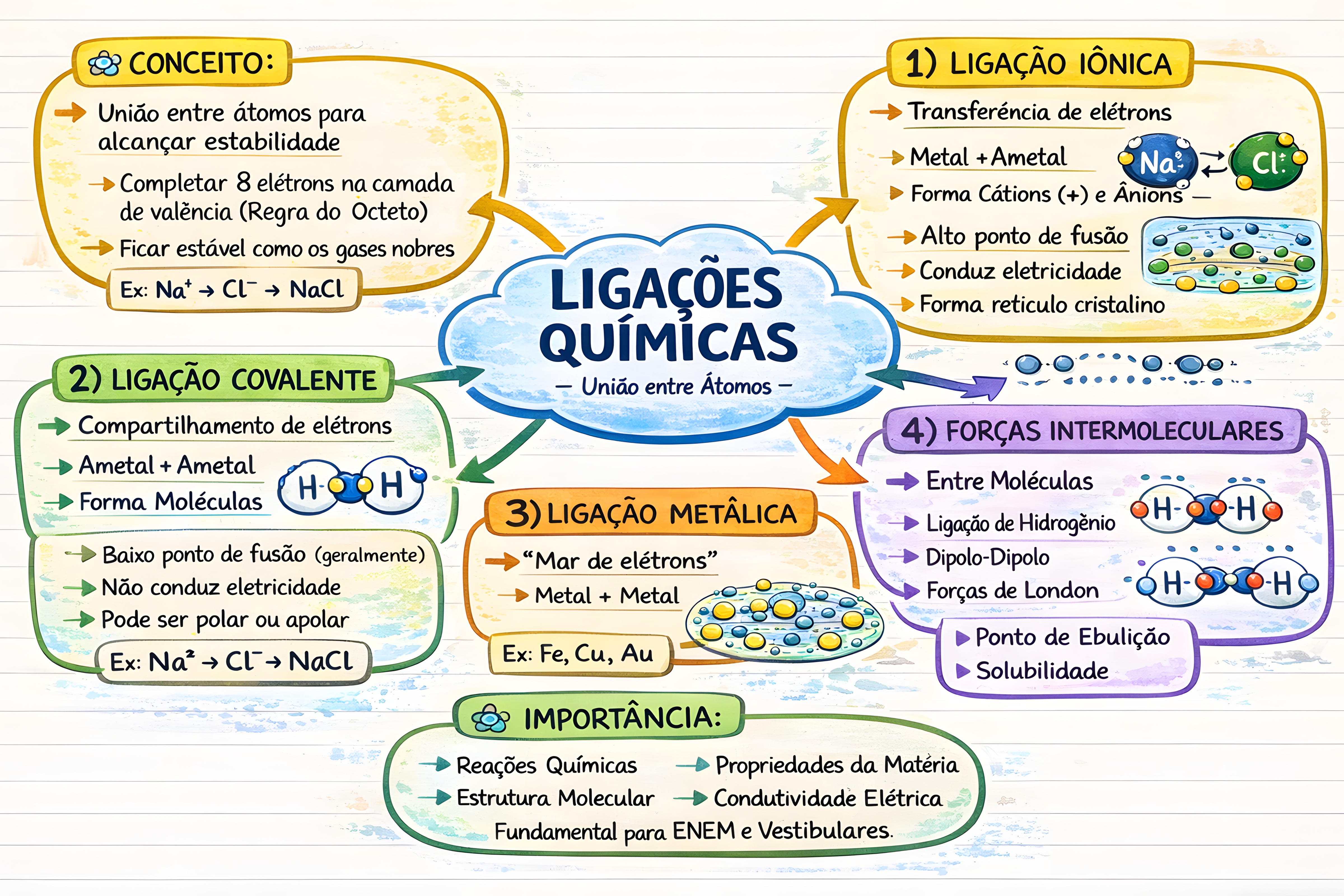
O estudo das ligações químicas é crucial para compreender a estrutura, as propriedades e a reatividade das substâncias. Desde a formação de moléculas simples como a água até a complexidade das macromoléculas biológicas, as ligações químicas são o alicerce da química e da vida, permitindo a formação de novos materiais e a ocorrência de reações que transformam o mundo ao nosso redor .