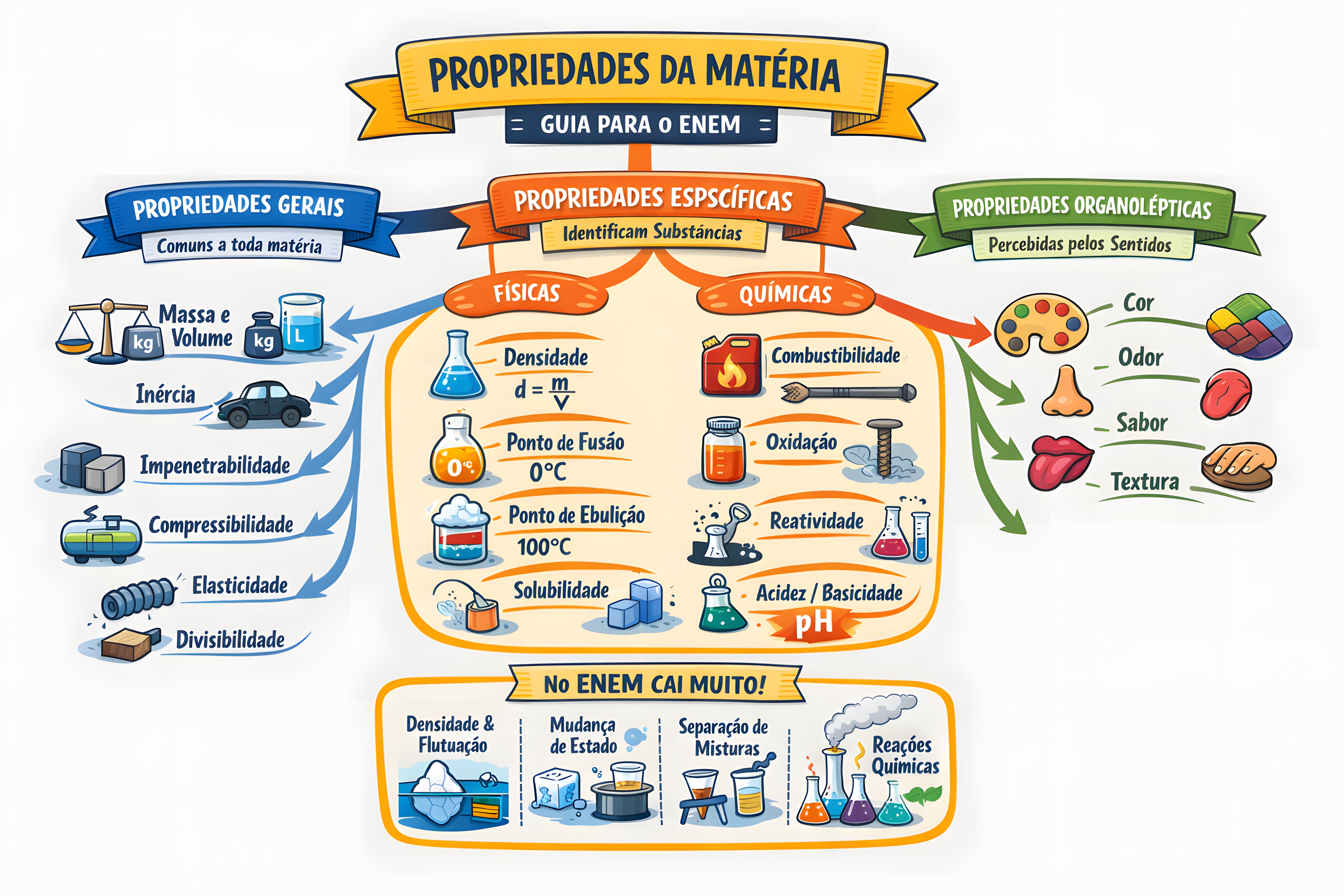
A matéria é tudo aquilo que possui massa e ocupa lugar no espaço. Compreender suas propriedades é fundamental para o estudo da Química e Física, sendo um tema recorrente e de grande importância para o Exame Nacional do Ensino Médio (ENEM). Este resumo aborda as principais características da matéria, suas classificações e como elas são abordadas nas provas.
O que é Matéria?
No contexto científico, a matéria é a substância física que compõe o universo observável. Ela pode ser encontrada em diferentes estados físicos (sólido, líquido, gasoso e plasma) e é formada por átomos e moléculas. As propriedades da matéria são as características que nos permitem identificar, diferenciar e descrever as substâncias.
Propriedades Gerais da Matéria
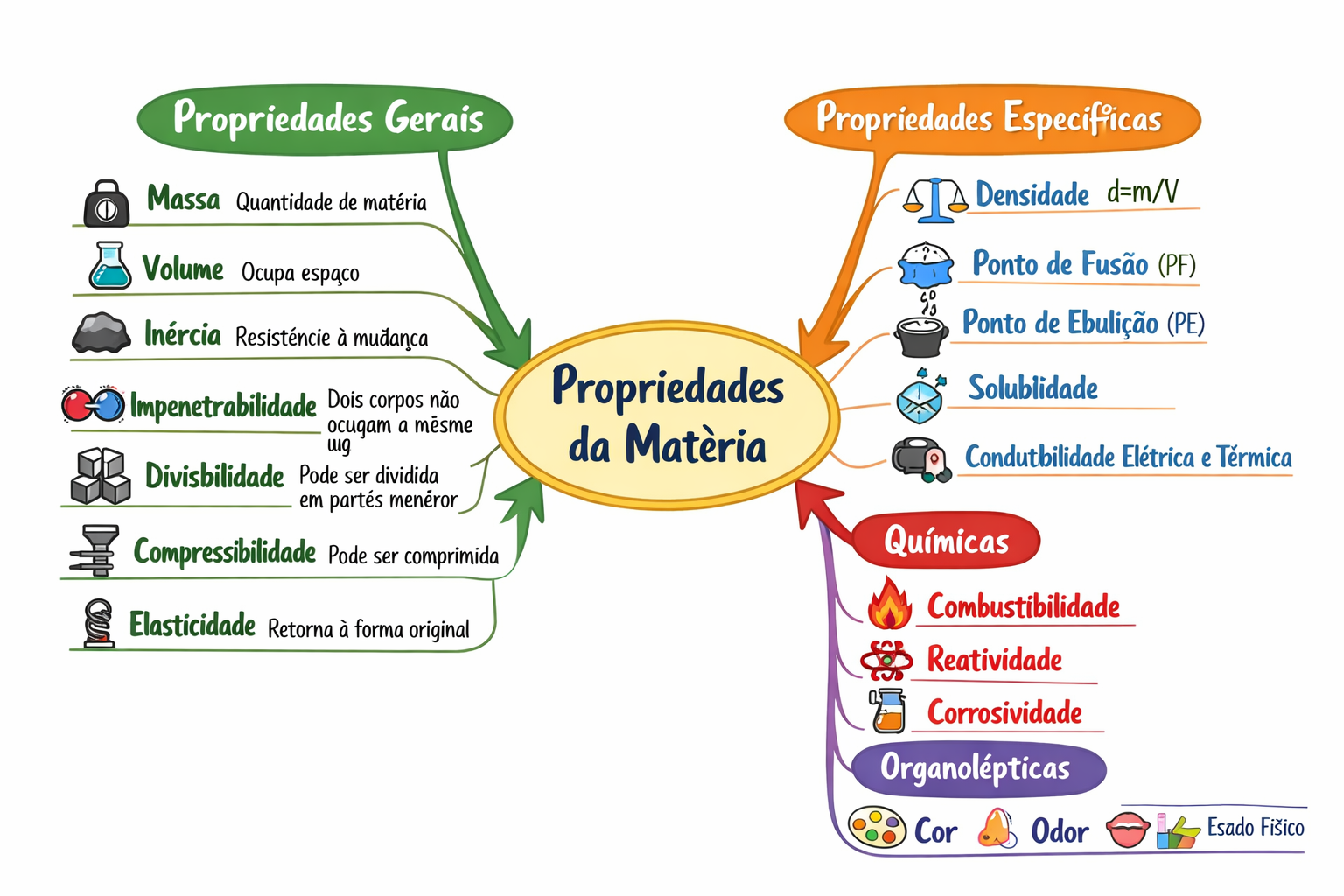
As propriedades gerais são aquelas que toda e qualquer matéria possui, independentemente de sua composição ou estado físico. Elas não permitem diferenciar uma substância da outra, mas são intrínsecas à sua existência.
- Massa: Quantidade de matéria presente em um corpo. É uma medida da inércia de um corpo.
- Volume: Espaço ocupado por um corpo. Pode ser medido em litros (L), mililitros (mL), metros cúbicos (m³) ou centímetros cúbicos (cm³).
- Inércia: Tendência de um corpo em manter seu estado de repouso ou de movimento retilíneo uniforme, a menos que uma força externa atue sobre ele. Quanto maior a massa, maior a inércia.
- Impenetrabilidade: Duas porções de matéria não podem ocupar o mesmo lugar no espaço ao mesmo tempo. Por exemplo, ao encher um copo com água, o ar que estava dentro é deslocado.
- Divisibilidade: A matéria pode ser dividida em partes cada vez menores, até atingir seus constituintes fundamentais (átomos).
- Compressibilidade: Capacidade da matéria de ter seu volume reduzido sob a ação de uma força externa. Gases são altamente compressíveis, enquanto líquidos e sólidos são pouco compressíveis.
- Elasticidade: Capacidade da matéria de retornar à sua forma e volume originais após a cessação de uma força que a deformou.
Propriedades Específicas da Matéria
As propriedades específicas são aquelas que permitem diferenciar uma substância da outra, pois são características de cada tipo de matéria. Elas são cruciais para a identificação de substâncias desconhecidas.
Propriedades Físicas
Relacionam-se com as características observáveis da matéria sem que haja alteração em sua composição química.
- Densidade: Relação entre a massa e o volume de uma substância (d = m/V). É uma das propriedades mais importantes para a identificação de substâncias.
- Ponto de Fusão (PF): Temperatura na qual uma substância passa do estado sólido para o líquido sob uma dada pressão. Para substâncias puras, o PF é constante.
- Ponto de Ebulição (PE): Temperatura na qual uma substância passa do estado líquido para o gasoso sob uma dada pressão. Para substâncias puras, o PE é constante.
- Solubilidade: Capacidade de uma substância (soluto) de se dissolver em outra (solvente) para formar uma solução.
- Condutibilidade Elétrica e Térmica: Capacidade de uma substância de conduzir eletricidade ou calor.
Propriedades Químicas
Descrevem a capacidade de uma substância de se transformar em outra, alterando sua composição química.
- Combustibilidade: Capacidade de uma substância de queimar na presença de um comburente (geralmente oxigênio), liberando energia.
- Reatividade: Tendência de uma substância de reagir quimicamente com outras substâncias.
- Corrosividade: Capacidade de uma substância de degradar materiais por meio de reações químicas.
Propriedades Organolépticas
São aquelas percebidas pelos nossos sentidos (visão, olfato, paladar, tato).
- Cor: Característica visual da substância.
- Odor: Cheiro da substância.
- Sabor: Gosto da substância (não deve ser testado em laboratório com substâncias desconhecidas).
- Estado Físico: Sólido, líquido ou gasoso à temperatura ambiente.
Mapa Mental: Propriedades Gerais e Específicas da Matéria
Para facilitar a visualização e memorização das propriedades da matéria, confira o mapa mental abaixo, que resume as propriedades gerais e específicas com seus respectivos subtópicos.
Estados Físicos da Matéria e Mudanças de Estado
A matéria pode se apresentar em diferentes estados físicos, que dependem da energia cinética de suas partículas e das forças de atração entre elas. Os três estados mais comuns são sólido, líquido e gasoso.
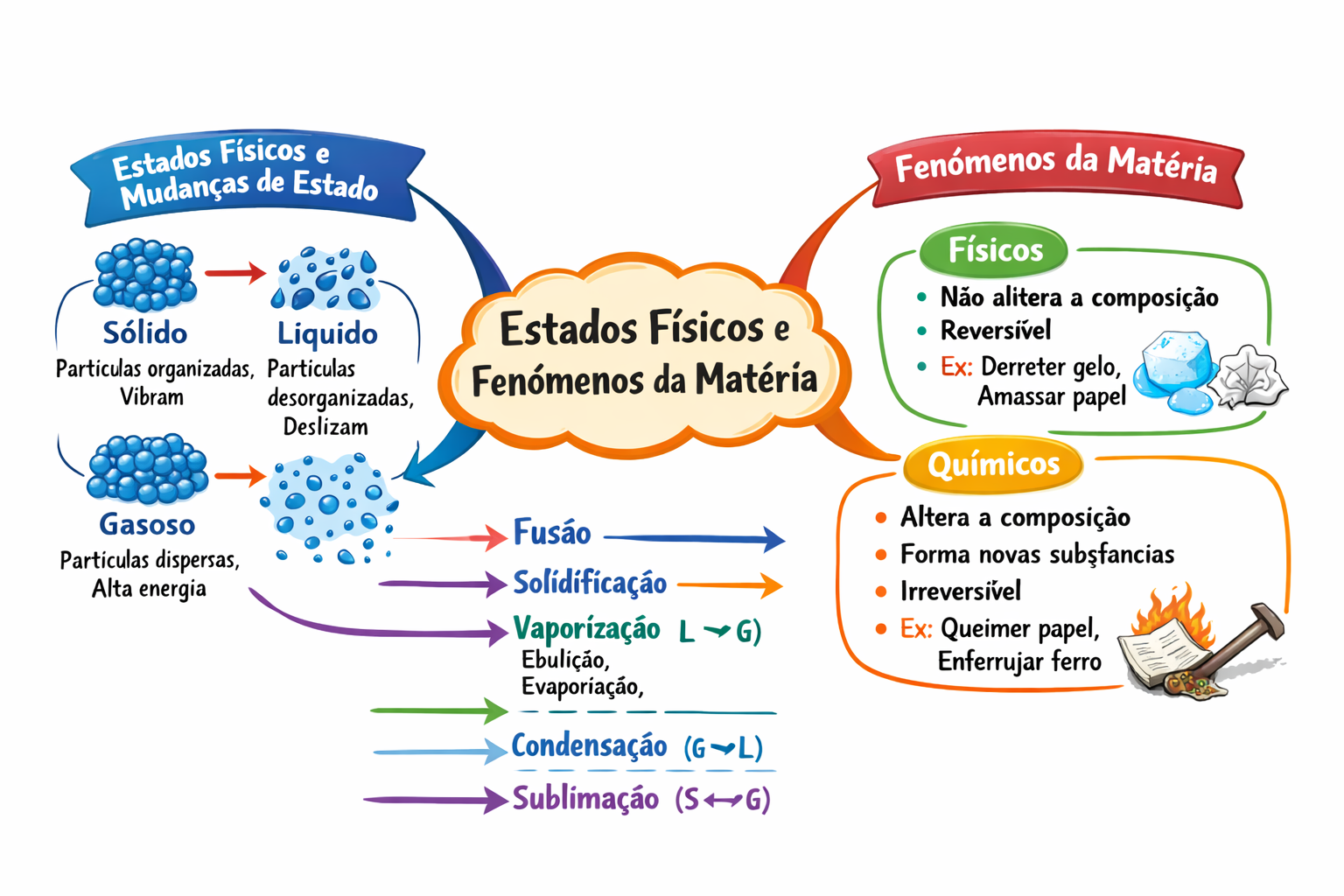
Sólido, Líquido e Gasoso
- Sólido: As partículas estão muito próximas e organizadas, com forte força de atração. Possuem forma e volume definidos, e as partículas apenas vibram em posições fixas.
- Líquido: As partículas estão mais afastadas e desorganizadas que no sólido, com forças de atração intermediárias. Possuem volume definido, mas forma variável (assumem a forma do recipiente), e as partículas deslizam umas sobre as outras.
- Gasoso: As partículas estão muito afastadas e desorganizadas, com forças de atração muito fracas. Não possuem forma nem volume definidos (ocupam todo o volume do recipiente), e as partículas se movem livremente e em alta velocidade.
Fusão, Vaporização, Solidificação, Condensação e Sublimação
As mudanças de estado físico ocorrem quando há alteração na temperatura e/ou pressão, levando a um ganho ou perda de energia pelas partículas da matéria.
- Fusão: Passagem do estado sólido para o líquido (ex: gelo derretendo).
- Solidificação: Passagem do estado líquido para o sólido (ex: água virando gelo).
- Vaporização: Passagem do estado líquido para o gasoso. Pode ocorrer de três formas:
- Evaporação: Lenta e natural, ocorre à temperatura ambiente (ex: roupa secando no varal).
- Ebulição: Rápida e com formação de bolhas, ocorre a uma temperatura específica (ponto de ebulição) (ex: água fervendo).
- Calefação: Instantânea, ocorre quando o líquido entra em contato com uma superfície muito quente (ex: gota d’água em chapa quente).
- Condensação (ou Liquefação): Passagem do estado gasoso para o líquido (ex: vapor d’água formando orvalho).
- Sublimação: Passagem direta do estado sólido para o gasoso, sem passar pelo líquido (ex: naftalina diminuindo de tamanho) ou vice-versa (resublimação ou deposição).
Fenômenos Físicos vs. Fenômenos Químicos
É crucial diferenciar os tipos de fenômenos que a matéria pode sofrer, pois isso indica se houve ou não alteração em sua composição.
- Fenômenos Físicos: São aqueles que alteram a forma, o tamanho ou o estado físico da matéria, mas não modificam sua composição química. A substância continua sendo a mesma. São geralmente reversíveis.
- Exemplos: Amassar um papel, derreter gelo, cortar madeira, dissolver açúcar em água, ferver água.
- Fenômenos Químicos: São aqueles que provocam uma alteração na composição química da matéria, resultando na formação de novas substâncias. São geralmente irreversíveis.
- Exemplos: Queimar papel, enferrujar um prego, cozinhar um alimento, a fotossíntese, a digestão de alimentos.
Como diferenciar na prova do ENEM?
No ENEM, a chave para diferenciar fenômenos é observar se houve formação de novas substâncias. Indicadores de fenômenos químicos incluem: mudança de cor, liberação de gás (efervescência), formação de precipitado (sólido no fundo do recipiente), liberação ou absorção de calor (aquecimento ou resfriamento espontâneo), e emissão de luz.
Mapa Mental: Estados Físicos e Fenômenos da Matéria
Visualize as transformações da matéria e a distinção entre fenômenos físicos e químicos com este mapa mental.
Como as Propriedades da Matéria caem no ENEM?
No ENEM, as questões sobre propriedades da matéria frequentemente envolvem a aplicação desses conceitos em situações do cotidiano ou em problemas que exigem a diferenciação de substâncias. Tópicos como densidade, pontos de fusão e ebulição, e a distinção entre fenômenos físicos e químicos são bastante cobrados. É comum a apresentação de gráficos de aquecimento e resfriamento para análise dos estados físicos e suas transições.
Exemplos de aplicação no ENEM:
- Cálculo de densidade para identificar materiais ou determinar volumes.
- Análise de gráficos de temperatura versus tempo para identificar substâncias puras ou misturas.
- Diferenciação entre processos de separação de misturas baseados nas propriedades físicas (ex: destilação, filtração).
- Identificação de reações químicas (propriedades químicas) em fenômenos naturais ou industriais.
Dicas de Estudo e Conclusão
Para dominar as propriedades da matéria para o ENEM, é essencial:
- Compreender os conceitos: Não apenas memorizar, mas entender o que cada propriedade significa e como ela se manifesta.
- Resolver exercícios: A prática leva à perfeição. Busque questões de provas anteriores do ENEM e de outros vestibulares.
- Relacionar com o cotidiano: Observe como as propriedades da matéria estão presentes no seu dia a dia (ex: gelo flutuando na água, cozimento de alimentos).
- Focar nas diferenças: Entender a distinção entre propriedades gerais e específicas, e entre fenômenos físicos e químicos, é crucial.
Dominar as propriedades da matéria é um passo importante para garantir um bom desempenho nas questões de Química e Física do ENEM. Com estudo e prática, você estará preparado para identificar e aplicar esses conceitos com confiança.