Regra do Octeto: O Guia Completo para Estabilidade Atômica
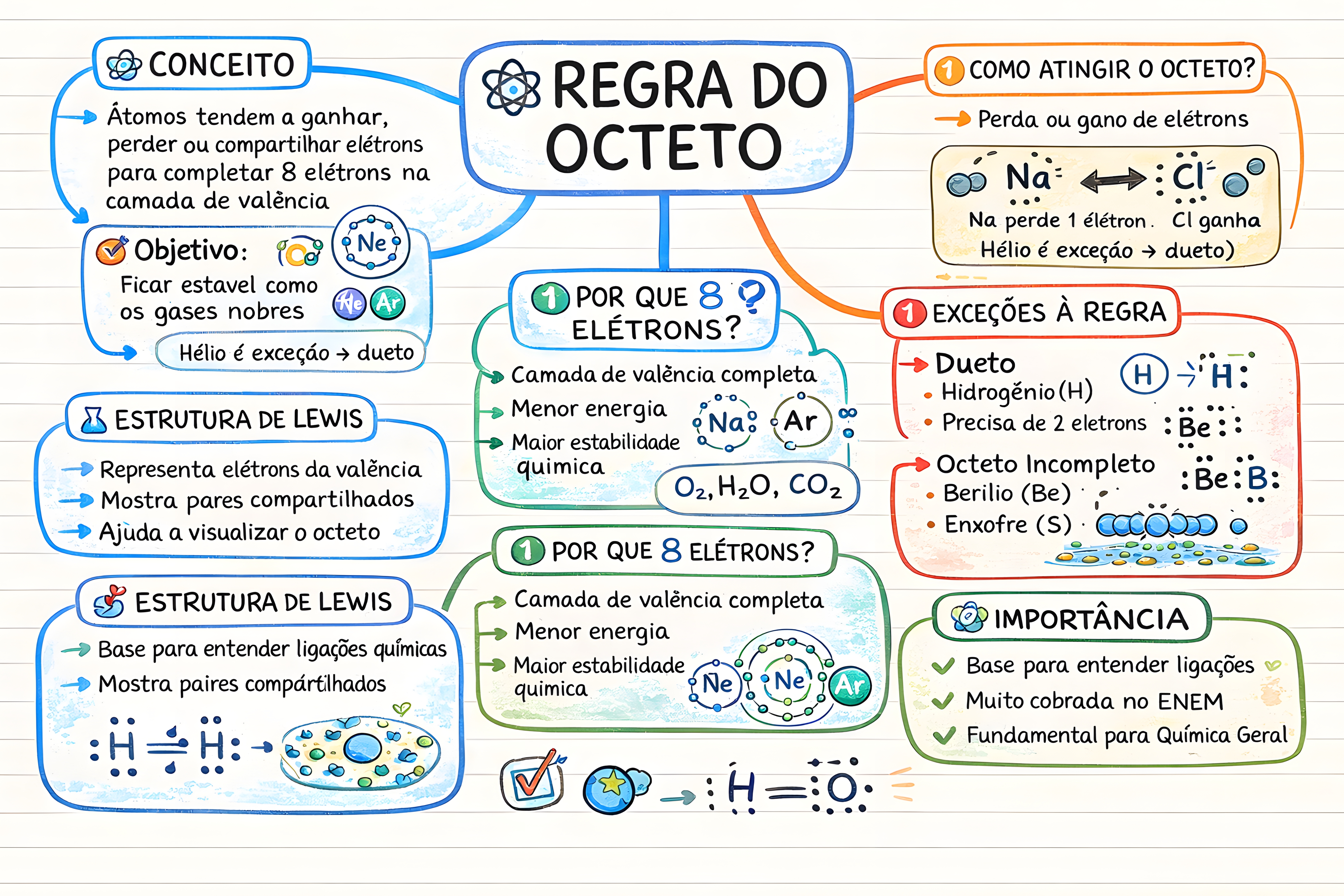
A Regra do Octeto, também conhecida como Teoria do Octeto, é um princípio fundamental da química que explica a tendência dos átomos em adquirir estabilidade química. Proposta por Gilbert Lewis em 1916, essa regra estabelece que os átomos buscam ter oito elétrons em sua camada de valência (a camada eletrônica mais externa) para alcançar a configuração eletrônica de um gás nobre, que são elementos quimicamente estáveis .
O que é a Regra do Octeto?
A essência da Regra do Octeto reside na observação de que os gases nobres (como Neônio, Argônio, Criptônio, etc.), com exceção do Hélio (que possui dois elétrons na camada de valência), apresentam oito elétrons em sua camada mais externa. Essa configuração lhes confere uma alta estabilidade e baixa reatividade. Os demais elementos da Tabela Periódica tendem a ganhar, perder ou compartilhar elétrons para atingir essa mesma configuração eletrônica e, assim, se estabilizar .
Como os Átomos Alcançam o Octeto?
Os átomos podem alcançar a estabilidade do octeto de três maneiras principais, formando ligações químicas:
•Ligação Iônica: Ocorre quando há transferência de elétrons entre átomos, geralmente entre um metal (que perde elétrons) e um ametal (que ganha elétrons). Ambos os íons resultantes adquirem a configuração de um gás nobre.
•Ligação Covalente: Ocorre quando há compartilhamento de elétrons entre átomos, tipicamente entre ametais. Os elétrons compartilhados contam para a camada de valência de ambos os átomos, permitindo que cada um atinja o octeto.
Exemplos Práticos da Regra do Octeto
Para ilustrar a aplicação da Regra do Octeto, vejamos alguns exemplos comuns:
| Molécula/Composto | Átomos Envolvidos | Como o Octeto é Alcançado | Representação |
| Cloreto de Sódio (NaCl) | Sódio (Na) e Cloro (Cl) | Na (metal) perde 1 elétron, tornando-se Na⁺ (configuração do Neônio). Cl (ametall) ganha 1 elétron, tornando-se Cl⁻ (configuração do Argônio). | Ligação Iônica |
| Gás Cloro (Cl₂) | Dois átomos de Cloro (Cl) | Cada átomo de Cloro compartilha 1 par de elétrons com o outro, totalizando 8 elétrons na camada de valência de cada um. | Ligação Covalente |
| Metano (CH₄) | Carbono (C) e Hidrogênio (H) | O Carbono compartilha 4 pares de elétrons com 4 átomos de Hidrogênio, atingindo 8 elétrons. Cada Hidrogênio atinge 2 elétrons (dueto). | Ligação Covalente |
Exceções à Regra do Octeto
Embora a Regra do Octeto seja uma ferramenta valiosa para prever a formação de ligações, é importante notar que existem exceções. Nem todos os átomos se estabilizam com exatamente oito elétrons na camada de valência. As principais exceções incluem :
1.Estabilização por Dueto: Átomos como o Hidrogênio (H), Lítio (Li) e Berílio (Be) tendem a se estabilizar com apenas dois elétrons na camada de valência, assemelhando-se ao Hélio. Por exemplo, na molécula de H₂, cada hidrogênio compartilha um par de elétrons, completando seu dueto.
2.Octeto Incompleto: Alguns elementos, especialmente os do Grupo 13 (como Boro e Alumínio), podem ser estáveis com menos de oito elétrons na camada de valência. Por exemplo, no trifluoreto de boro (BF₃), o boro possui apenas seis elétrons em sua camada de valência, mas a molécula é estável.
3.Expansão do Octeto: Elementos a partir do terceiro período da Tabela Periódica (como Fósforo, Enxofre e Cloro) possuem orbitais d vazios que podem ser utilizados para acomodar mais de oito elétrons na camada de valência. Isso permite que formem mais de quatro ligações. Exemplos incluem o pentacloreto de fósforo (PCl₅) e o hexafluoreto de enxofre (SF₆), onde o átomo central possui 10 e 12 elétrons, respectivamente.
4.Número Ímpar de Elétrons (Radicais Livres): Moléculas que possuem um número ímpar de elétrons na camada de valência não podem satisfazer a Regra do Octeto para todos os átomos. Um exemplo é o óxido nítrico (NO), que possui um elétron desemparelhado, tornando-o um radical livre.
Importância da Regra do Octeto na Química
Apesar das exceções, a Regra do Octeto continua sendo um conceito central no estudo das ligações químicas e da estrutura molecular. Ela fornece uma base simplificada e eficaz para prever a reatividade e a geometria de muitas moléculas, sendo uma ferramenta didática essencial para estudantes de química em todos os níveis. Compreender a Regra do Octeto é o primeiro passo para desvendar a complexidade das interações atômicas e moleculares que regem o universo da química.







